একটি s অরবিটাল এবং দুটি p অরবিটাল সংমিশ্রিত হয়ে তিনটি সমশক্তিসম্পন্ন নতুন অরবিটাল উৎপন্ন হওয়ার প্রক্রিয়াকে sp সংকরণ বা sp2 Hybridization বলে।
কার্বন পরমাণুর ইলেকট্রন বিন্যাস নিম্নরূপ
C(12) 1s2 2s2 2px1 2py1 2pz (সাধারণ অবস্থায়)।
C (0) – 182 1s1 2px1 2py1 2pz1 (উত্তেজিত অবস্থায়)
sp2 সংকর অরবিটাল তিনটি একই সমতলে অবস্থান করে এবং পরস্পরের সাথে 120° কোণে উৎপন্ন করে। sp2 সংকর অরবিটাল গঠনের পর প্রত্যেক কার্বনের একটি করে 2p2 অরবিটাল অসংকরিত বা বিশুদ্ধ অবস্থায় থাকে। প্রত্যেকটি sp সংকর অরবিটালে 33.3% S চরিত্র ও 66.7% p চরিত্র থাকে।
ইথিলিন (HC2 = CH2) অণু গঠনকালে কার্বন পরমাণুদ্বয়ের প্রত্যেকটির একটি করে sp2 সংকর অরবিটাল পরপর অধিক্রমণ করে একটি sp2 sp2 (C-C) সিগমা বন্ধন সৃষ্টি করে। পরে প্রতিটি কার্বন পরমাণুর অবশিষ্ট দুটি করে মোট চারটি sp2 সংকর অরবিটালের প্রতিটির সাথে একটি করে H পরমাণুর 1s অরবিটালের অধিক্রমণ দ্বারা চারটি sp2 – s (C – H) সিগমা বন্ধন সৃষ্টি হয়। অসংকরিত 2p2 অরবিটালের লোব দুটি সমতলের উপরে ও নীচে পরস্পর সমান্তরালভাবে অবস্থান করে এরা পাশাপাশি অধিক্রমণের মাধ্যমে কার্বন-কার্বন বন্ধন গঠন করে।
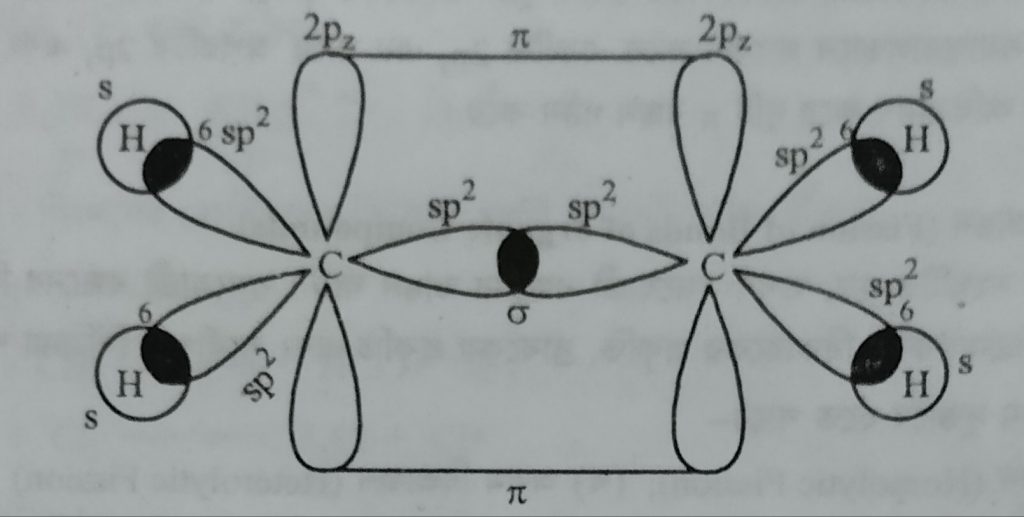
ইথিলিন অনুর অরবিটাল চিত্র।